硫氧化途径驱动北京城市大气硫酸盐气溶胶稳定硫同位素组成的变化
近日,本课题组研究成果《Roles of Sulfur Oxidation Pathways in the Variability in Stable Sulfur Isotopic Composition of Sulfate Aerosols at an Urban Site in Beijing, China》于2020年10月发表在Environmental Science & Technology-Letters杂志,使用硫同位素对北京重污染过程中大气硫酸盐的形成机制进行研究。耶鲁-南京信息工程大学大气环境中心博士生范美益为第一作者,章炎麟教授为通讯作者,该研究得到国家重点研发计划(2017YFC0212704)、江苏省自然科学基金(BK20180040)和江苏省双创团队支持。
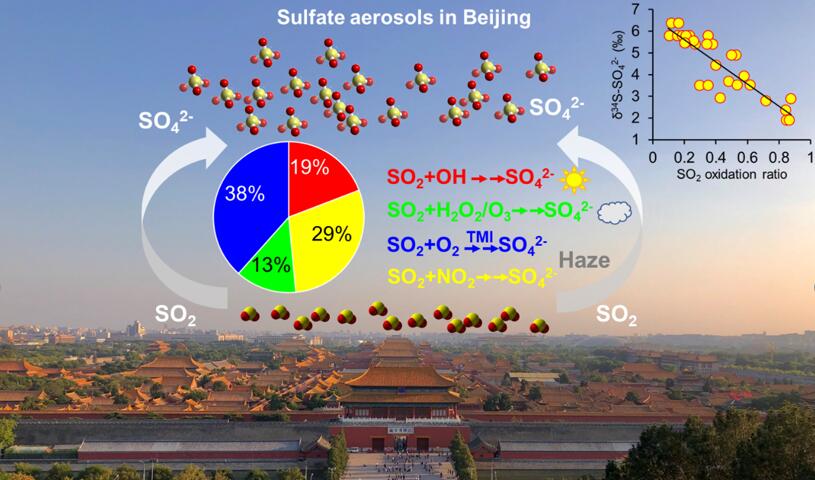
硫酸盐(SO42-)是大气气溶胶中重要的化学组分,对大气化学过程和气候变化具有重要影响。硫酸盐气溶胶可由人为和自然源直接排放,或通过气体到颗粒的二次转化生成。煤燃烧、工业排放、汽车尾气和生物质燃烧被认为是硫酸盐的主要来源。此外,海洋和内陆湿地土壤中的生物硫(如二甲基硫醚DMS、硫化氢H2S等)也是大气硫酸盐的重要来源,特别是在高温地区或微生物活性较高的季节。
大气中,硫酸盐气溶胶主要由SO2氧化生成,目前已知的氧化途径主要包括液相和气相(光化学)反应。气相反应过程中,SO2与OH反应生成气态H2SO4;气态H2SO4粘附在气溶胶粒子的表面,或在有利条件下(如高湿度)成核形成新粒子,增加气溶胶数浓度和云凝结核(CCN),这对直接和间接辐射都有影响;另一方面,气态H2SO4立即与NH3反应生成硫酸盐气溶胶。对于在云雾或烟雾中的水相反应,SO2溶解成液滴生成S(Ⅳ)( [SO2H2O] + [HSO3–] + [SO32-]),随后S(Ⅳ)与溶解的氧化剂,如过氧化氢(H2O2)、臭氧(O3)、O2(金属(TMI)催化条件下)和二氧化氮(NO2)反应生成硫酸盐气溶胶。
然而不同氧化途径对硫酸盐生成的相对贡献取决于多种因素,如光化学氧化和水相氧化的氧化剂浓度、气溶胶中液态水含量(ALWC)和酸度(pH)。因此,由于这些因素在不同污染条件下的较大差异,影响了不同氧化途径中SO2的反应速率,很难通过化学动力学计算来评估这些氧化途径的贡献。氧同位素(如δ18O和∆17O)经常用于确定硫酸盐气溶胶的形成机制。此外,研究表明硫同位素δ34S受来源变化的控制;然而,其也被用来量化从SO2到SO42-的不同氧化途径的相对贡献。
本研究利用稳定硫同位素(δ34S)值和贝叶斯模型对北京大气不同污染时期的硫酸盐(SO42-)来源进行定量解析,结果表明各污染源的贡献在不同污染时期基本保持不变(图1)。并且δ34S-SO42-与温度(R=-0.46,p<0.05)、湿度(R=-0.76,p<0.01)和SO2氧化率(SOR)(R=-0.88,p<0.01)均呈显著负相关(图2),说明硫酸盐的δ34S值取决于不同的SO2氧化过程。根据瑞利蒸馏定律和不同氧化途径的分馏系数(图3),我们定量解析了冬季采样期间一次硫酸盐、OH、H2O2/O3、NO2和O2(TMI催化)途径对硫酸盐生成的贡献,分别为7 %, 20 %, 16 %, 27 %和30 %。此外,根据不同时期的硫酸盐生成的结果(图4),TMI和NO2途径的贡献分别从清洁大气时期的24 % 和20 %增加到灰霾时期的38 %和29 %。研究结果表明TMI催化的O2和NO2氧化的SO2是北京冬季灰霾污染期间硫酸盐生成的主要途径。
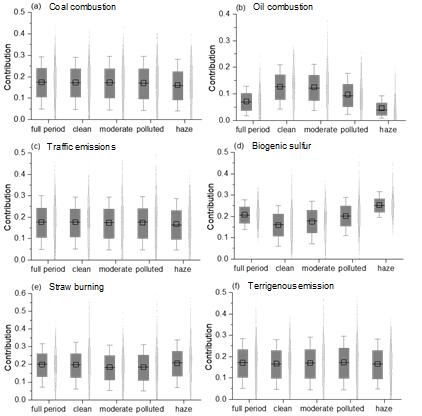
图1 不同污染水平下,燃煤、重油燃烧、交通排放、生物硫、秸秆燃烧和陆源排放对于硫酸盐气溶胶的相对贡献。
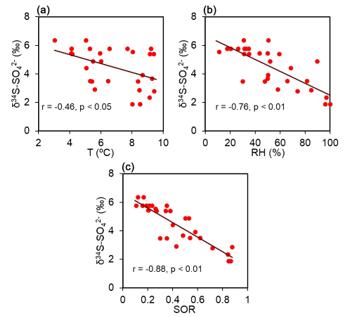
图2 δ34S-SO42- 与温度(T)(a)、相对湿度(RH)(b)和SO2氧化率(SOR)(c)的相关关系。
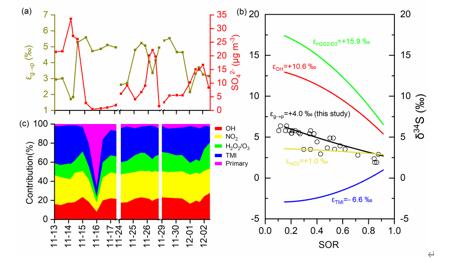
图3(a)采样期间模型估算分馏系数(ɛg→p)(棕黄点线),硫酸盐(SO42-)浓度(红色点线);(b)不同氧化途径(OH、H2O2/O3、NO2、TMI)产生的分馏系数;(c)不同氧化途径(OH、H2O2/O3、NO2、TMI)及一次硫酸盐(primary sulfate)对硫酸盐生成的贡献。
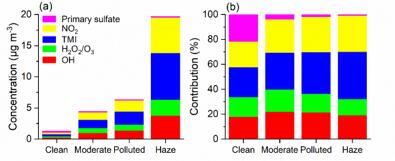
图4 不同污染时期一次硫酸盐和不同氧化途径(OH、H2O2/O3、NO2、TMI)生成的硫酸盐浓度(a)和相对贡献(b)。
文章链接:https://dx.doi.org/10.1021/acs.estlett.0c00623
